
「どう変わる!? がんとの向き合い方」をテーマに2回のトークセッションを実施し、ゲノム研究や人工知能(AI)によって大きく変わろうとしているがん医療について、今後の展望や社会的な課題について考えました。
第1回 「どう変わる!? がんとの向き合い方──ゲノム研究で広がる可能性」 2020年2月16日(日)
https://www.miraikan.jst.go.jp/events/2020021695.html
第2回 「どう変わる!? がんとの向き合い方──人とAIでひらく新たな医療」 2020年3月8日(日)ニコニコ生放送
https://www.miraikan.jst.go.jp/events/2020030894.html
この記事では、がん医療における人工知能(AI)の可能性について取り上げた第2回のトークセッションから、特にAIに関連する話題を中心に紹介します。
〔企画・ファシリテーター:科学コミュニケーター 鎌田芽生〕
※記事の最後に、イベント動画へのリンクを掲載しています。
※当日の詳しい内容とアンケート結果等は、文末に掲載するリンクから科学コミュニケーターブログをご参照ください(本記事は、ブログの内容をまとめてご紹介しています)。
はじめに
トークセッションでは、共催の文部科学省新学術領域研究「システム癌新次元」より3名のゲストスピーカーをお迎えしました。
宮野悟氏(東京大学医科学研究所ヒトゲノム解析センター センター長、「システム癌新次元」代表)
山口類氏(愛知県がんセンター研究所 システム解析学分野 分野長)
中田はる佳氏(国立がん研究センター 社会と健康研究センター 生命倫理・医事法研究部 研究員)

宮野悟氏

山口類氏

中田はる佳氏
イベント当日の話は、以下のような流れで進みました。
(1)医学や生物学にとどまらない、がん研究プロジェクト「システム癌新次元」
(2)人とAIが協調する新たながんゲノム医療に向けて
(3)日本で未承認薬を使う制度とその課題
(4)アンケートとディスカッション
この中から、この記事ではAIに関わる(2)と(3)の話を中心に紹介し、さらにそれに関する視聴者アンケートとディスカッションを紹介します。
大量のゲノムのデータ、どうやって処理する?
がん研究プロジェクト「システム癌新次元」の代表でもある宮野さんから、「がん」とDNAからなる遺伝情報である「ゲノム」との関係について、概要をお話しいただきました。がんは、ゲノムが何らかの影響により変異することで引き起こされる疾患です。しかし、ゲノムの変異が見つかっても、その変異ががんを引き起こしているのかどうかという「解釈」や、変異に対してどのような治療が可能なのかという「医療翻訳」はまだ十分とはいえません。例えば、イギリスのデータベースには約3000万のがんの変異と約26000の論文が人の手で紐づけられており、医療現場ではこれらのデータからいちいち検索しているそうです。そして、当初はがんの原因ではないと思われていた変異も、研究が進むことである種のがんでは原因であったことが分かってくるなど、新しい情報が加わることでこれらのデータの解釈が正しくなくなることもあり、これらの膨大なデータを扱うことは、もはや人間の手に負える量ではなくなってきているというのです。
このような現状でがん研究を進めるために、膨大なデータに立ち向かうためのAIやスパコンといった情報学の研究と、遺伝情報を扱うことから課題になってきそうなELSI(倫理的・法的・社会的問題)の研究を融合したがん研究プロジェクト「システム癌新次元」を立ち上げ、研究を進めているということです。
そこでまず、ゲノムのデータを使って有用な情報を抽出するAIのお話を、山口氏にしていただきました。この研究の背景には、一人ひとりのゲノムの配列を読む技術(シークエンス解析)の進歩があります。
人とAIが協調する新たながんゲノム医療へ向けて
シークエンス解析を担うシークエンサーという機械の性能が良くなったことで、大量のゲノムのデータを安価に得られるようになりました。しかし、問題は、そこから得られたあまりにも膨大なデータから変異を探し出すという作業。これは例えるならば大量に積み上げられた本の束をシュレッダーにかけて、出てきた断片から間違いを探していくくらいの出来事なのだとか…!とても人間の手には負えそうにありません。

ここで登場するのが、スーパーコンピューター!
東京大学医科学研究所にある、ゲノム解析に特化したスパコン「SHIROKANE」を使うことで、短時間で大量のデータの解析が可能になるのです。
次の図はスパコンでの変異の検出例です。シークエンス解析で得られた灰色の断片のようなゲノム情報が、ヒトゲノムのどこに当てはまるのかを探し出し、同じような場所での変異が多数見られる場所を検出しています。
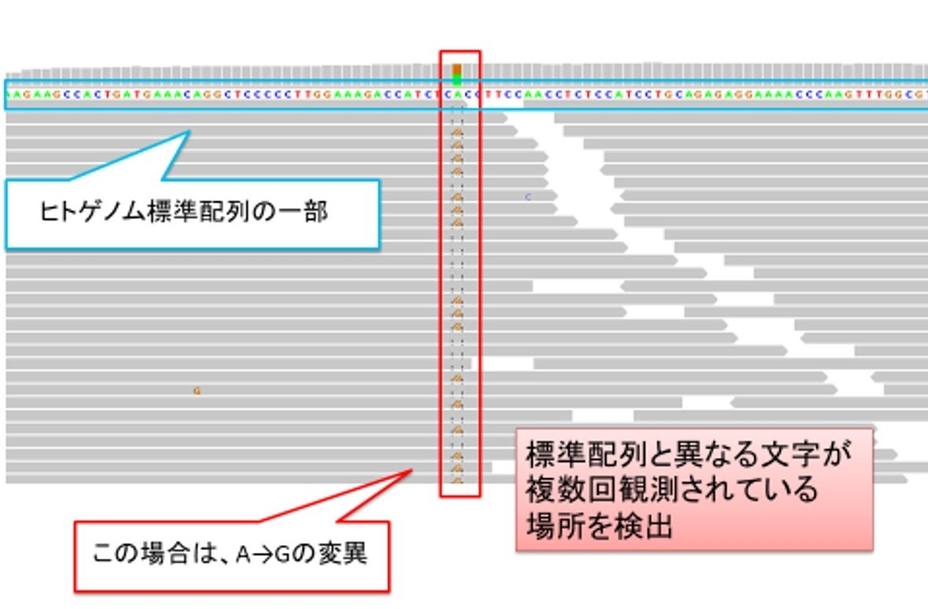
こうして、ゲノムのデータがたくさん得られるようになり、基礎研究が進んでくると、次はゲノムのデータを使って患者さんの治療に役立てるということが重要になります。患者さんのゲノムのデータから変異を探し出し、変異の情報からどのような治療法が有効であるかを提案し、実際の医療現場へ戻すという「臨床シークエンス」が実現しつつあるのです。
その一例として16124個のゲノムの変異から原因遺伝子を発見、治療へ結びつけられたという事例もありました。
ゲノムのデータの「解釈」と「翻訳」がボトルネックに
しかし、臨床シークエンスを行ううえで、変異がどのような意味を持ち、どう治療へ役立てられるのかという、シークエンスデータの「解釈」と「翻訳」がボトルネックになっています。
そこで登場するのがAIなのです。
「Watson for Genomics」というがんに特化したAIでは、得られたゲノムの変異に対して、その変異がどのような意味を持つのか、データベースや論文で調べる作業をAIが代わって実施をします。この作業を人の手で行うと2週間かかりますが、AIを使って行うとなんとたったの2分!
そしてAIの提案でがんを克服した事例もありました。急性白血病の治療を行ってもなかなか改善しなかった患者さんについて、AIで治療薬を検索した結果、違う種類の白血病であったことが判明! AIの提案に則った治療を行った結果、白血病を克服することができました。
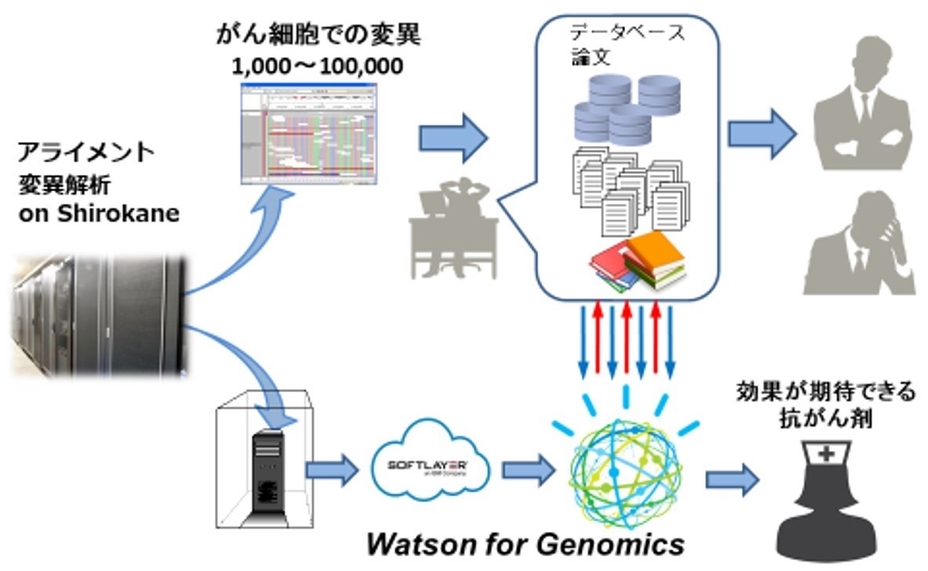
得られたゲノムの変異について、AIを使って治療へ役立てていきます。
AIで提案された治療法は保険適用されているものばかりではなく、時には治験中の薬剤なども提案されることがあります。
例えば、ゲノムのどこに変異があるかすでにわかっている、大腸がんの細胞株を使ってAIによる治療法の探索を行った際に、4237個あるゲノムの変異の中からがんに関わると考えられる12個の変異を見つけ出しました。そしてこれらに合う治療法として、保険適用されている治療法だけでなく、現在治験中の薬剤、さらには大腸がんでは承認されていないものの他のがんでは承認されている薬剤の治療法も提案されたのです。
AIと医師とが協調することでより良い医療へ
AIが医療の場に入ってくると、人間の医師はいなくなってしまうのでしょうか?こんな声をたまに耳にします。ですが、AIは医師にとって代わるものではなく、医師と協調することでより良い医療につながっていくのだと山口氏はおっしゃいます。例えば、転移性乳がんの画像診断において、病理医の誤診率が3.5%、AIの誤診率は7.5%ありました。しかしAIが診断したものを病理医が確認することで、誤診率は0.5%まで下がったのです! AIと医師とが協調して医療を行っていく、そんな希望にあふれた未来がありそうです。
そしてAIが使われることで医師の負担が少なくなる分、医師は患者さんとのコミュニケーションに時間を取ることが可能になります。治療方針や治療に関する悩みなど、今まで以上に丁寧にコミュニケーションを取りながら一緒に考えることができるようになるかもしれません。
しかし、AIを活用して治療へ役立てるこの技術もまだまだ開発途上の段階です。全ゲノム遺伝情報のうち、遺伝子と呼ばれて、身体のなかでさまざまな働きをするタンパク質という分子をつくる部分は約2%に過ぎません。この遺伝子に変異があればできあがってくるタンパク質にも変異が生じることがあるので、がんとの関連も比較的研究が進んでいます。ですがゲノムの残りの約98%の領域については、まだまだ分からないことだらけです。こうした領域が治療に対して重要な役割を持つかどうかもまだ分かりません。これを調べるためには、まだまだデータが足りません。患者さんのデータのみならず、健康な人のデータもまだまだ足りない状況なのです。これらのデータをどのように集めて、また得られた結果をどのように還元していくかがこれからの課題なのだということをお話していただきました。
山口氏のお話の中で、承認されていない薬剤についてもAIで提案されたという事例がありました。では、実際の医療現場では承認されていない「未承認薬」を使う制度はあるのでしょうか? それについて中田氏に伺いました。
日本で未承認薬を使う制度とその課題
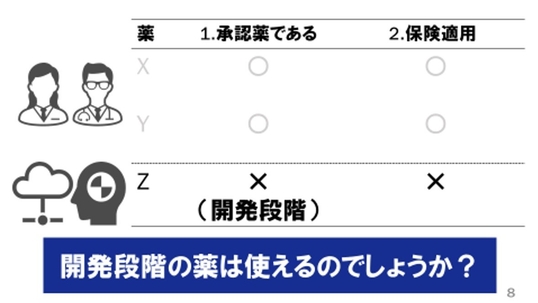
病院で使われている薬のほとんどは、①安全性や有効性が確認されていて、薬が国に認められていること(承認)、②国民のお金で薬代が安くなること(保険適用)の2つの条件を満たしています。
通常、医師が患者さんに処方するのはこうした薬ですが、開発段階の薬を使いたいと思ったとき、使うことはできるのでしょうか?
開発段階の薬を使うには、大きく下記の3つの方法があります。
(1) 治験
(2) 拡大治験
(3) 患者申出療養制度
(1) 治験
新薬候補が薬として認められ、たくさんの人に使ってもらうには、国に安全性や有効性を示すデータを提出する必要があります。治験は、そのデータを集めるために行われます。
例えば、参加者には新薬候補と既存薬のいずれかを使ってもらい、その効果や副作用を比べることでデータを集めていきます。
ただし治験の参加には条件があり、体の状態や決められた人数、決められた病院などでしか実施ができません。希望しても治験に参加できないことがあります。
(2) 拡大治験
試してみたい新薬候補の治験はあっても、患者さんが治験の条件にあわなかった場合にこの制度を使うことができます。
医師から製薬会社に治験の参加枠を広げてもらえるよう依頼し、製薬会社が了承した場合に制度を利用できます。
(3) 患者申出療養制度
試してみたい新薬候補について、日本で治験をやっていなかった場合にこの制度を使うことができます。
患者が新薬候補を試したい希望を医師に申し出、医師は製薬企業と相談して研究計画を作成し、製薬会社が了承した場合に制度を利用できます。
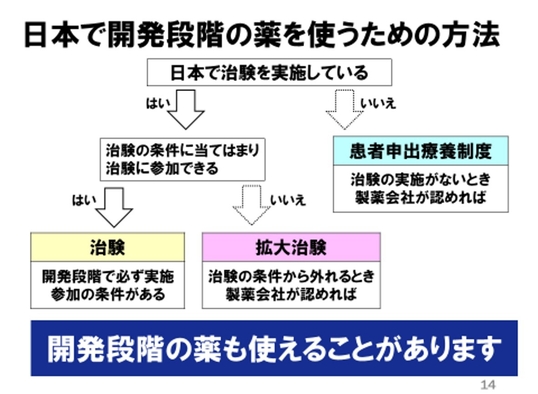
この3つの制度は、「現在治験を実施しているか」「治験の条件に当てはまるか」によって、右のように使い分けられることになります。
このように、治療の選択肢として未承認薬も入ってくることになるのです。
選択肢が広がることは一見良いことに思えるのですが、果たしてそればかりなのでしょうか?
例外制度で未承認薬を使えることは、良いことばかりとは限らない

例外制度で未承認薬を使うことについて、次のような課題が挙げられます。
(1) 新薬候補を使えるかどうかは製薬企業次第
製薬企業側には例外制度で未承認薬を提供する法律上の義務はありません。
未承認薬を提供したい気持ちはあっても、ビジネスとして成り立たせるためには必要以上の未承認薬を製造する余裕がない可能性もあります。また、使用人数が増えたり、条件の異なる人が加わったりすることで新たな副作用がわかってしまうと承認へ結びつけることが難しくなることもあるのです。
(2) 本当に自分に効果があるのだろうか?
効果が全く期待できないものは、例外制度があっても試すことはできません。また、ヒトでの実績がなく、動物で試したデータしかない場合もあります。
そして、効果が期待できる一方で、副作用が起こることもあるかもしれません。
(3) 費用はだれが負担する?
開発段階の薬の費用については、例外制度では患者へ全額請求することができます。これらの薬はもちろん保険適用外です。
例えば、開発段階の治療法として、腹膜播種や進行性胃がんに対する抗がん剤の使用に約29万円かかります。重症心不全で開発中の人工心臓を使用する例では1600万円もかかることもあるといいます。
(4) みんなが平等に使える?
例外制度の利用に関する課題はまだあります。特定の病院でしか行えない、そもそも情報を得るのが難しいなどがあります。
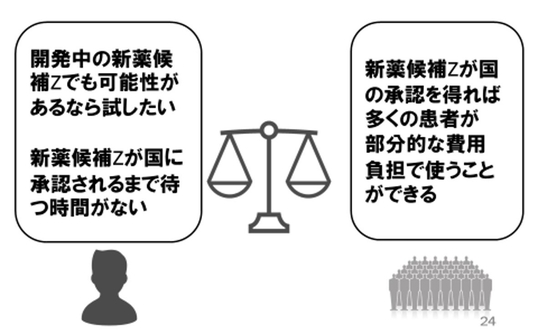
また、もし患者さんの多くが例外制度を使うようになり、治験に参加する患者さんが少なくなると、新薬候補の承認が遅れ、保険適用される新薬として使えるようになるまでにさらに時間がかかることもあるかもしれません。
個人の希望と集団の利益とのバランスを、あなたならどのように考えるでしょうか。
アンケートとディスカッション
トークセッション後半では、オンラインでアンケートを行いながらディスカッションしました。ここでは、AIによる治療法の提案に関する視聴者アンケートの結果とそれに対するゲストスピーカーのコメントをご紹介します。
AIが治療法を提案することについての質問を視聴者へ投げかけました。
Q1. あなたががん患者であったとして、AIに治療薬の提案をしてほしいと思いますか?
①提案してほしい:80.2%
②提案してほしくない:6.2%
③どちらともいえない:13.6%
Q2. AIに治療薬を「提案をしてほしい」「どちらともいえない」と答えた方へお聞きします。そう思ったのはなぜでしょうか?
①治療の選択肢が広がるから:56.5%
②AIの提案の精度が高そうだから:14.5%
③短時間で治療薬をみつけられるから:11.6%
④医師の負担が減りそうだから:7.2%
⑤AIの発展、医療の発展のため:5.8%
⑥その他:4.3%
Q3. AIに治療薬を「提案をしてほしくない」「どちらともいえない」と答えた方へお聞きします。そう思ったのはなぜでしょうか?
①新しい情報がAIに入っていないから:12.0%
②自分の遺伝情報を提供することに抵抗感があるから:20.0%
③医師の経験による勘の方が信用できるから:12.0%
④誤診のときの責任の所在があいまいだから:40.0%
⑤心に寄り添った提案をしてもらえないから:0%
⑥その他:16.0%

責任の所在はあいまいなのか?
宮野氏 「国から承認されている医療機器については製作者に責任があります。しかし、AIは医療の支援という位置づけにあり、最終判断、すべての責任はあくまで医師にあります。このような通知が平成30年(2018年)に厚労省から行われております」
高額な薬を提案されたら困る
山口氏 「今のところ薬の価格を考慮したAIは見たことがありません。価格を含めて薬の選択肢を絞り込んでいくのは医師や患者さんなど、治療に関わる人間で行っていくことになるので、心配はしなくてもよいのかなと思います」
AIを使いこなせる臨床医はいる?
宮野氏 「AIを使いこなす臨床医はどんどん増えてきています。自分でAIの開発を試みる臨床医もいます」
AIが治療薬を提案するためには、AIの判断材料となる情報が必要となります。そこで、AIへの個人情報の提供に関して聞きました。
Q4. AIから治療薬の提案を受けるために、病歴や遺伝情報などの自分の情報を提供する必要があります。あなたは、自分の情報を提供しても良いと思いますか?
①提供してもよい:68.0%
②提供したくない:12.0%
③どちらともいえない:20.0%
Q5. AIから治療薬の提案を受けるために、病歴や遺伝情報などの自分の情報を提供することについて、心配なことはありますか?
①個人情報が守られるのか不安:66.7%
②知りたくないことまでわかってしまうから:20.0%
③なんとなくイヤ:4.4%
④その他:8.9%
保険に入りにくくなる?
山口氏 「アメリカには遺伝情報の内容によって保険の入りやすさを変えてはいけないという法律があるのです」
宮野氏 「日本では法整備がされていません。ただ、がん保険の条件に『今までにがんにかかったことのない人』などの条件が付くことがあります。アメリカでは遺伝子差別禁止法がありますが、日本では差別をしないという考え方がベースにあるため、同様の法律が作りにくいという面もあります。一方でゲノム情報を活用して健康医療を活性化するような法律、強力化法案は考えられたりしていました」
がん患者のゲノムを調べて予想外の変異が見つかったとき、患者や家族へのフォローはどうなっている?
中田氏 「病院で遺伝医療に関する診療科があると、認定遺伝カウンセラーがいる場合もあります。遺伝カウンセラーと話し合いをして家族に共有をするかどうかを決めることになります」
宮野氏 「医療現場では、このような予期せぬ発見があると(患者さんにお伝えするかどうか)、非常に悩み考えて答えを出しているのです。ただ、遺伝カウンセラーは日本ではまだ200人強ほどしかおらず、遺伝カウンセラーの仕事のみで生活ができる状況ではありません。一方でアメリカでは、遺伝カウンセラーが専門職として活躍しているのです」
情報が売買される未来になる?
宮野氏 「国や地域によってはあり得ると思います。薬の開発のために効率よくゲノム情報を集めたいとなると、そのように使われることはあるかもしれません。私たちがゲノム情報の提供に関して同意を受けるときに、同意書に利用目的として何が書かれているかを確認する必要があります」
中田氏 「ヨーロッパのある国では、ゲノム情報を集めて別の国へ売るという戦略を取っていたところがありました。日本では、検査の際に遺伝情報の提供に関してその後の研究のために利用をしてもよいかという確認があります。もちろんこれは医療の発展のための研究ではありますが、一歩間違えると情報の売買になるのではと心配する人もいます」
さて、ここまでイベントの内容を抜粋してご紹介してきました。
AIを使うことで医療の発展が期待される一方で、そこに至るまでには課題もまだまだあります。また、立場によってはAIからの提案に対する選択も変わりうる中で、一つの結論を出すことはとても難しいでしょう。
今や2人に1人はがんにかかると言われている中で、自分や周りの人がいつがんにかかってもおかしくはありません。自分が当事者になったときの将来のがん医療について、このイベントで少しでも考えることができたなら幸いです。
イベント動画:ニコニコ生放送
本イベントはニコニコ生放送でタイムシフト視聴が可能です。コメントの入力はできませんが、どなたでも無料でご覧いただけます。
https://live2.nicovideo.jp/watch/lv324605284
関連ブログ
企画・ファシリテーション

トークセッションを終えて
科学コミュニケーター 鎌田芽生(かまた・めい)
今回のイベントは、新型コロナウイルス感染予防のためニコニコ生放送での実施となりましたが、予定していた2時間を大幅に延長するほどたくさんのコメントをいただき、一緒に考えてもらうことができました。本当にありがとうございました。
少し前まで、がんは、患者本人に告知すべきかどうかという議論もあったほど、罹ったら最後、というイメージが強い疾患でした。しかし、がんの治療は目まぐるしく進歩しており、治療法や治療薬の開発がどんどん進められています。今回ご紹介した技術も、少し先の未来には当たり前になっているものかもしれません。私たちが当事者になったときに、がんの治療をどのように選択するか、考える良い機会となったなら幸いです。
